广西专用2020版高考化学二轮复习专题能力训练4化学反应速率与化学平衡含解析
专题能力训练4 化学反应速率与化学平衡
(时间:45分钟 满分:100分)
一、选择题(共7小题,每小题8分,共56分。每小题只有1个选项符合题意)
1.乙二醇制备原理为CH3OOC—COOCH3(g)+4H2(g)HOCH2—CH2OH(g)+2CH3OH(g)
ΔH=-34 kJ·mol-1,下图表示一定温度下,达到平衡时乙二醇的产率随原料投料比[n(氢气)n(草酸二甲酯)]和压强的变化关系,其中三条曲线分别表示体系压强为1.5 MPa、2.5 MPa、3.5 MPa的情况,下列说法中正确的是( )
A.原料投料比[n(氢气)n(草酸二甲酯)]增大,平衡常数K增大
B.原料投料比[n(氢气)n(草酸二甲酯)]越大,乙二醇的产率越小
C.升高温度后,v(正)>v(逆)
D.曲线丙对应的压强p(丙)=1.5 MPa
答案:D
解析:温度不变,原料投料比[n(氢气)n(草酸二甲酯)]增大,平衡常数K不变,A项错误;由图像可知,一定范围内原料投料比[n(氢气)n(草酸二甲酯)]越大,乙二醇的产率越大,B项错误;该反应正向放热,升高温度,平衡向逆反应方向移动,故v(正)
0,在一定条件下可自发进行,则必须是熵增反应,即ΔS>0,错误。
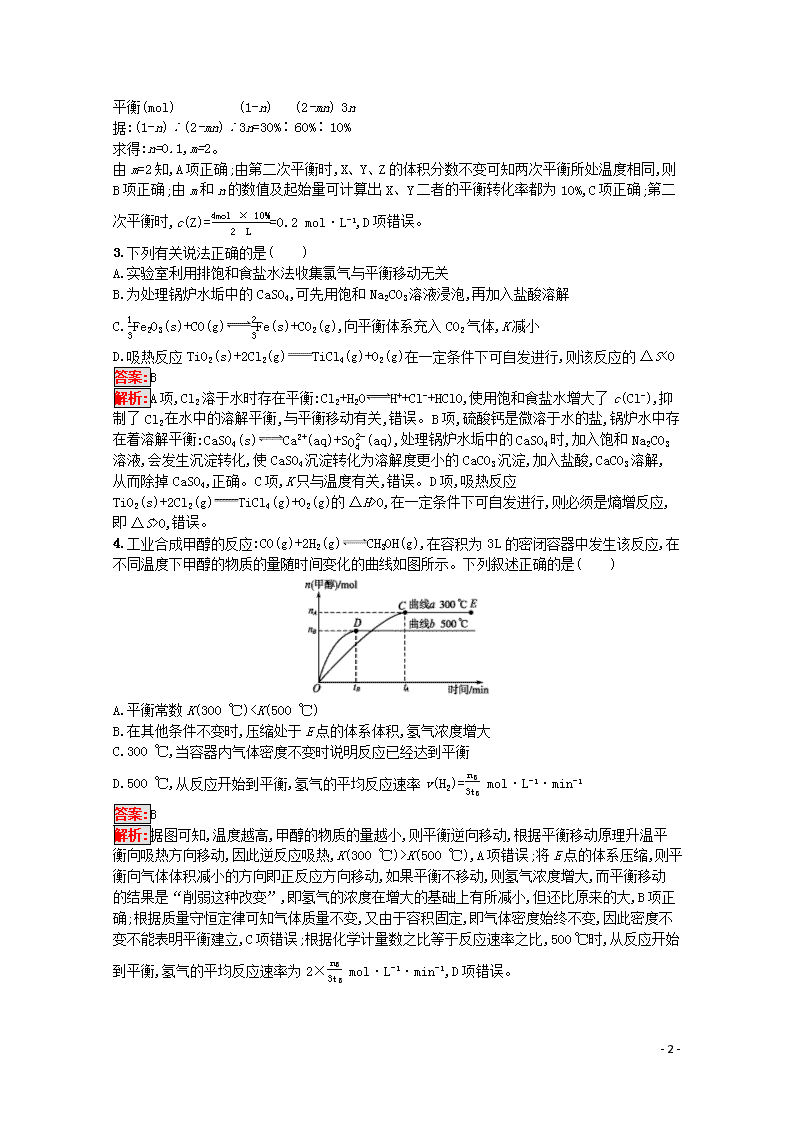
4.工业合成甲醇的反应:CO(g)+2H2(g)CH3OH(g),在容积为3 L的密闭容器中发生该反应,在不同温度下甲醇的物质的量随时间变化的曲线如图所示。下列叙述正确的是( )
A.平衡常数K(300 ℃)K(500 ℃),A项错误;将E点的体系压缩,则平衡向气体体积减小的方向即正反应方向移动,如果平衡不移动,则氢气浓度增大,而平衡移动的结果是“削弱这种改变”,即氢气的浓度在增大的基础上有所减小,但还比原来的大,B项正确;根据质量守恒定律可知气体质量不变,又由于容积固定,即气体密度始终不变,因此密度不变不能表明平衡建立,C项错误;根据化学计量数之比等于反应速率之比,500 ℃时,从反应开始到平衡,氢气的平均反应速率为2×nB3tB mol·L-1·min-1,D项错误。
5.(2018河北衡水模拟)某温度下,反应2A(g)B(g) ΔH>0,在密闭容器中达到平衡,平衡后c(A)c(B)=a,若改变某一条件,足够时间后反应再次达到平衡,此时c(A)c(B)=b,下列叙述正确的是( )
- 6 -
A.在该温度下,保持容积固定不变,向容器内补充了B气体,则ab
答案:B
解析:A项,补充B气体后平衡时压强变大,正反应程度变大,c(A)c(B)变小,即a>b;B项,充入B气体,新平衡状态与原平衡等效,c(A)c(B)不变,即a=b;C项,升温,平衡右移,c(A)c(B)变小,即a>b;D项相当于减压,平衡左移,c(A)c(B)变大,即a”或“<”),得出该结论的理由是 。
- 6 -
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ⅱ补充完整。
ⅰ.SO2+4I-+4H+S↓+2I2+2H2O
ⅱ.I2+2H2O+ + +2I-
(4)探究ⅰ、ⅱ反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
序号
A
B
试剂组成
0.4 mol·L-1 KI
a mol·L-1 KI
0.2 mol·L-1 H2SO4
实验现象
溶液变黄,一段时间后出现浑浊
溶液变黄,出现浑浊较A快
序号
C
D
试剂组成
0.2 mol·L-1 H2SO4
0.2 mol·L-1 KI
0.000 2 mol I2
实验现象
无明显现象
溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快
①B是A的对比实验,则a= 。
②比较A、B、C,可得出的结论是 。
③实验表明,SO2的歧化反应速率D>A,结合ⅰ、ⅱ反应速率解释原因: 。
答案:(1)3SO2(g)+2H2O(g)2H2SO4(l)+S(s)
ΔH=-254 kJ·mol-1
(2)> 反应Ⅱ是气体分子数减小的反应,温度一定时,增大压强,化学平衡正向移动,H2SO4的物质的量分数增大
(3)SO2 4H+ SO42-
(4)①0.4 ②I-是SO2歧化反应的催化剂,且在H+存在下,催化速率增大;但H+单独存在时,不具有催化作用 ③反应ⅱ比反应ⅰ快,增大I2的浓度,反应ⅱ的反应速率增大,H+浓度增大,加强了I-的催化能力
解析:(1)由题给示意图可知,反应Ⅱ为二氧化硫发生歧化反应生成硫酸和硫,反应的化学方程式为3SO2(g)+2H2O(g)2H2SO4(l)+S(s),由盖斯定律可知,-(反应Ⅲ+反应Ⅰ)得反应Ⅱ,则ΔH=-(ΔH3+ΔH1)=-(-297 kJ·mol-1)-(+551 kJ·mol-1)=-254 kJ·mol-1,则热化学方程式为3SO2(g)+2H2O(g)2H2SO4(l)+S(s) ΔH=-254 kJ·mol-1。(2)反应Ⅱ为气体分子数减小的反应,增大压强,化学平衡正向移动,硫酸的物质的量分数增大,则p2大于p1。(3)由题意可知,I-为反应的催化剂,则反应ⅱ的反应物为I2、SO2和水,生成物为氢碘酸和硫酸,反应的离子方程式为I2+SO2+2H2O4H++2I-+SO42-。(4)①A与B是探究H+浓度对反应速率的影响,因此A和B中KI溶液浓度必须相同,则a为0.4;②对比A、B、C的实验现象可知,I-是SO2歧化反应的催化剂,且在H+存在下,催化速率增大;但H+单独存在时,不具有催化作用;③对比A、D实验现象可知,增大I2的浓度,反应ⅱ的反应速率增大,H+浓度增大,加强了I-的催化能力。
- 6 -
9.(24分)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)CH3OH(g) ΔH1=-99 kJ·mol-1
②CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol-1
③CO2(g)+H2(g)CO(g)+H2O(g) ΔH3=+41 kJ·mol-1
回答下列问题:
(1)反应①的化学平衡常数K表达式为 ;图1中能正确反映平衡常数K随温度变化关系的曲线为 (填曲线标记字母),其判断理由是 。
图1
图2
(2)合成气组成n(H2)n(CO+CO2)=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示,α(CO)值随温度升高而 (填“增大”或“减小”),其原因是 ;图2中的压强由大到小为 ,其判断理由是 。
答案:(1)K=c(CH3OH)c(CO)·c2(H2)[或Kp=p(CH3OH)p(CO)·p2(H2)]
a 反应①为放热反应,平衡常数数值应随温度升高变小
(2)减小 升高温度时,反应①为放热反应,平衡向左移动,使得体系中CO的量增大;反应③为吸热反应,平衡向右移动,又使产生CO的量增大;总结果,随温度升高,使CO的转化率降低
p3>p2>p1 相同温度下,由于反应①为气体分子数减小的反应,加压有利于提升CO的转化率;而反应③为气体分子数不变的反应,产生CO的量不受压强影响。故增大压强时,有利于CO的转化率升高
解析:(1)反应①的K表达式为c(CH3OH)c(CO)·c2(H2)。
因反应①为放热反应,所以平衡常数应随温度升高而变小,所以选a。
(2)升高温度,反应①平衡向左移动,使体系中n(CO)增大;反应③为吸热反应,平衡向右移动,又使产生n(CO)增大;总结果是随温度升高,CO的转化率降低。
- 6 -
因为相同温度下,由于反应①为气体分子数减小的反应,加压有利于增大CO的转化率;反应③为气体分子数不变的反应,压强改变对平衡不产生影响。所以压强增大,CO转化率升高,在图2中,同一温度下,CO转化率高的对应压强大,则p3>p2>p1。
- 6 -