- 2021-07-05 发布 |
- 37.5 KB |
- 12页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
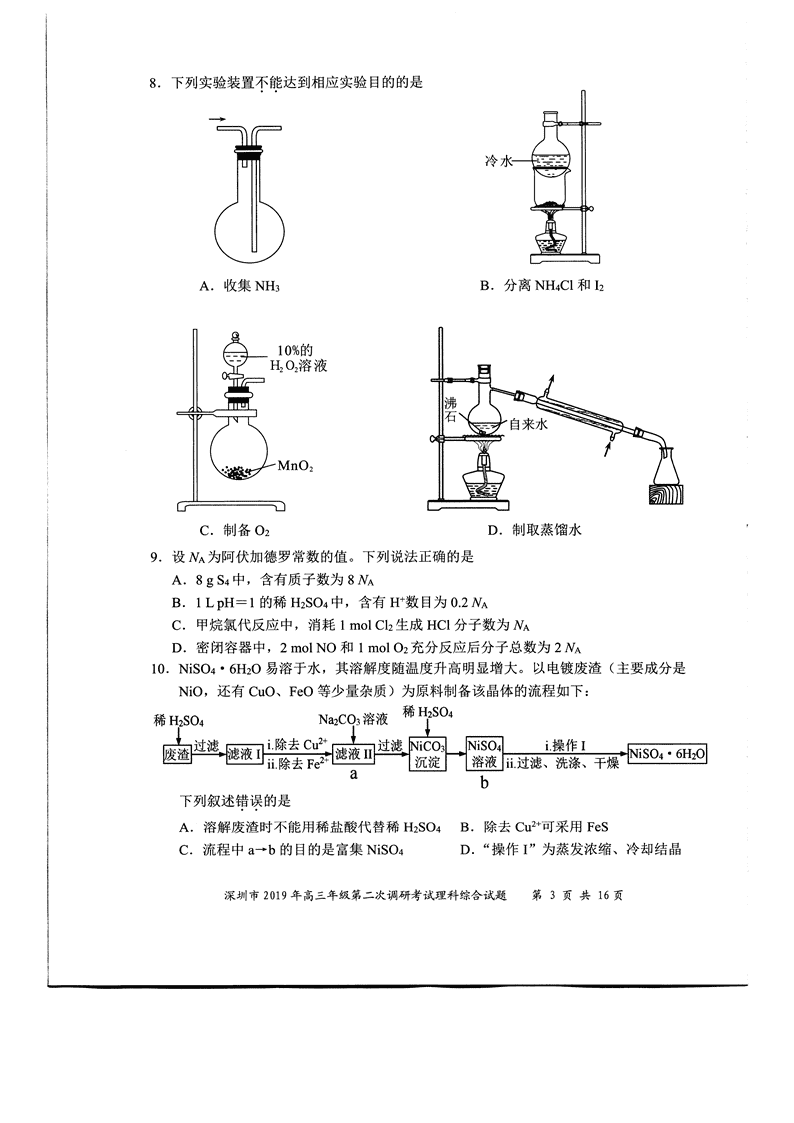
广东省深圳市2019年高三年级第二次调研考试化学试题
化学部分 2019 年深圳市高三年级第二次调研考试化学参考答案及评分标准 7 8 9 10 11 12 13 B B C A B C D 26.(15 分) (1)①圆底烧瓶(1 分) ②h,i→d,e(1 分,有错不得分) g,f→b(c) (1 分,有错不得分) ③未升华出来的 FeCl3 与未反应完的铁粉在水溶液中反应生成 Fe2+(2 分)(或答“气 态 FeCl3 会分解成 FeCl2 和 Cl2”,给 2 分;若答“K3[Fe(CN)6]与铁粉反应生成 Fe2+”、 “HCl 气体未除尽,与 Fe 反应生成 FeCl2”给 1 分;若答“氯气与铁粉反应生成 FeCl2”不得分) (2)①SO2+2Fe3++2H2O=4H++SO2− 4 +2Fe2+(2 分)(配平错误扣 1 分,反应物或生成物书写 错误不得分) ②Fe(OH)3 胶体(1 分) ③生成蓝色沉淀(1 分) ④<(2 分) <(2 分) ⑤增强 FeCl3 溶液的酸性(2 分)(答“减小 FeCl3 溶液的 pH”,“滴加浓盐酸”等合 理答案均给分) 27.(14 分) (1)Fe(OH)3(2分) (2)2Cr(OH)3+3H2O2+4KOH=2K2CrO4+8H2O(2分)(配平错误扣1分,反应物或生成 物书写错误不得分) (3)分解除去过量H2O2(2分)(答“防止H2O2在酸性条件下将Cr2O2− 7 还原”等合理答案均 给分) (4)2×10−8 mol•L −1(2分)(漏写或误写单位扣1分,数值错误不得分) (5)88.20%(答“0.882”、“ 88.2%”得2分,答“0.88”、“ 88%”得1分)(2分) (6)①C6H5OH+11H2O-28e−=6CO2↑+28 H+(2分)(配平错误扣1分,反应物或生成物 书写错误不得分,漏写“↑”不扣分) ②减小(2分) 28.(14 分) (1)①△H1+△H2-2△H3(2 分) ②B(2 分) (2)①16%(或 0.16)(2 分) 4.4×10−4(或 0.00044)(2 分) 1.54×10 −2(或 0.0154)(1 分) ②4×104(或 40000)(2 分) ③增大反应物的压强(答“增大反应物的浓度”、“增大压强”均得分)( 1 分) 提高反应物的压强,化学反应速率加快(2 分) 35.【化学——选修 3:物质结构与性质】(15 分) (1) (不写 3d、4s 扣 1 分)(2 分) (2)亚铜离子核外电子处于稳定的全充满状态(答“亚铜离子核外电子处于稳定的全充满 状态”也得分)( 2 分) (3)面心立方最密堆积(1 分) 12(1 分) (4)sp3 (1 分) N>O>C (1 分) 正四面体(1 分) PO3− 4 、ClO− 4(答 BF- 4 、SiF4、CCl4、SiO4− 4 也得分,其它合理答案均得分)( 2 分) (5)CaO 的晶格能大于 BaO 的晶格能(2 分) (6)397×1021 2 2NAa3(答“197+3×64+8 ( 2a×10−7) 3NA ”也得分)(2 分) 36.【化学——选修 5:有机化学基础】(15 分) (1)苯乙烯(1 分) 取代反应(1 分) (2)羟基、羧基(出现错误答案不得分)(2 分) 氢氧化钠水溶液(或“氢氧化钠溶液)”(1 分)加热(或“△”)(1 分) (3) + 2Cu(OH)2 △+ NaOH Cu2O↓ + 3H2O CHO OCH3 OCH3 + COONa OCH3 OCH3 (2 分)(配平错误扣 1 分,反应物或生成物书写错误不得分,漏写“↓”不扣分) (4)11(2 分) CH=CHCOOH OHHO 、 OHHO CH=CHCOOH (各 1 分,共 2 分) (5)CH3CH=CH2 HBr 过氧化物 CH3CH2CH2Br CH3CH2CH2OH CH3CH2CH=CHCOOH △ NaOH CH3CH2CHO △ O2/Cu 吡啶,△ H2C COOH COOH ( 3 分 , 第 1 步 1 分,第 2 、 3 步 共 1 分,第 4 步 1 分 ; 若 写 成 CH3CH=CH2 CH3CH2CH2OH CH3CH2CH=CHCOOH 催化剂/△ H2O CH3CH2CHO △ O2/Cu 吡啶,△ H2C COOH COOH 扣 1 分)查看更多