- 2021-07-05 发布 |
- 37.5 KB |
- 41页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019高考化学高分突破二轮复习专题十四氮及其化合物课件(41张PPT)
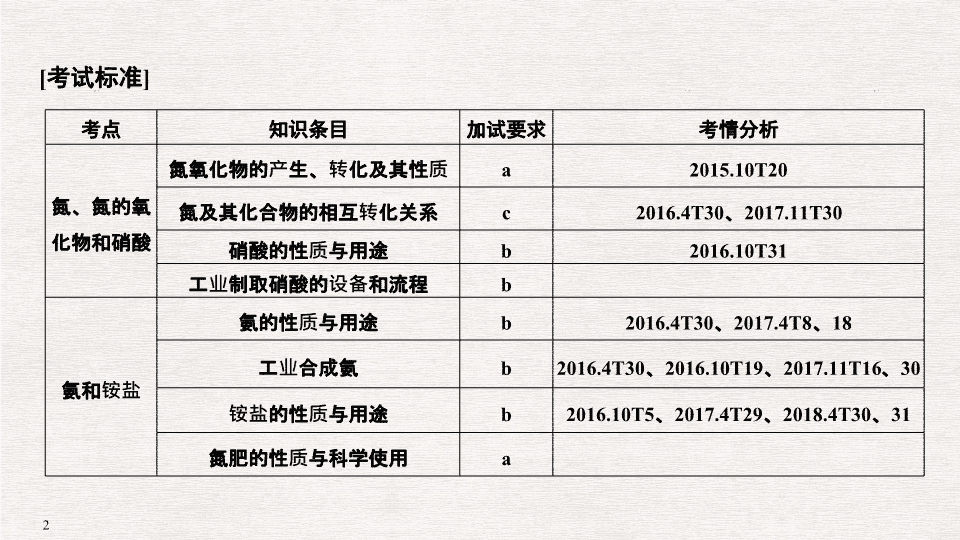
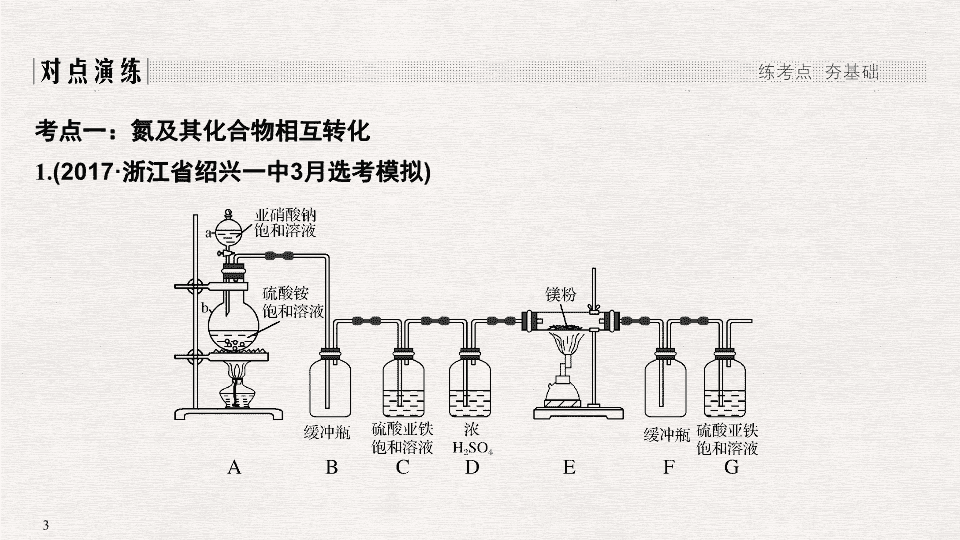
专题十四 氮及其化合物 ( 加试 ) [ 考试标准 ] 考点 知识条目 加试要求 考情分析 氮、氮的氧化物和硝酸 氮氧化物的产生、转化及其性质 a 2015.10T20 氮及其化合物的相互转化关系 c 2016.4T30 、 2017.11T30 硝酸的性质与用途 b 2016.10T31 工业制取硝酸的设备和流程 b 氨和铵盐 氨的性质与用途 b 2016.4T30 、 2017.4T8 、 18 工业合成氨 b 2016.4T30 、 2016.10T19 、 2017.11T16 、 30 铵盐的性质与用途 b 2016.10T5 、 2017.4T29 、 2018.4T30 、 31 氮肥的性质与科学使用 a 考点一:氮及其化合物相互转化 1. (2017· 浙江省绍兴一中 3 月选考模拟 ) 回答下列问题: (1) 检查装置气密性的方法是 __________________________________________ , a 的名称是 ________ , b 的名称是 ________ ; (2) 写出 NaNO 2 和 (NH 4 ) 2 SO 4 反应制备氮气的化学方程式 ___________________________________________________________ ; (3)C 的作用是 ________________________ , D 的作用是 ________________________ ,是否可以把 C 和 D 的位置对调并说明理由 ___________________________ ; (4) 写出 E 中发生反应的化学方程式 ________________ ; (5) 请用化学方法确定是否有氮化镁生成,并检验是否含有未反应的镁,写出实验操作及现象 ___________________________________________________________ 。 考点二:氮的氧化物 2. (2018· 浙江桐乡高级中学月考 ) 用下列装置制取并收集 NO 2 气体,其中最合理的是 ( ) 解析 铜与浓硝酸反应的产物是 NO 2 ,其密度比空气的大,因此应利用向上排空气法收集 NO 2 气体,导气管应长进短出,这样才能将装置中的空气排尽,保证收集到的气体纯净,只有 C 项符合。 答案 C 考点三:氨气的性质 3. (2018· 浙江嘉兴学科基础测试 ) 实验室制取少量干燥的氨气涉及下列装置,其中正确的是 ( ) A. ① 是氨气发生装置 B. ② 是氨气吸收装置 C. ③ 是氨气发生装置 D. ④ 是氨气收集、检验装置 解析 NH 4 Cl 固体受热分解生成 NH 3 和 HCl ,而当温度降低时, NH 3 和 HCl 又重新化合成固体 NH 4 Cl ,气体进入干燥管的机会不多, ① 错误;氨气极易溶于水按照装置图会发生倒吸, ② 错误;向 CaO 中滴加浓氨水, CaO 遇水生成 Ca(OH) 2 ,同时放出大量热量,使浓氨水中的氨气逸出, ③ 正确;装置中试管口处应塞一团棉花,氨气易溶于水防止与空气对流,得不到纯净的氨气, ④ 错误。 答案 C 考点四:氨气的实验室制法 4. (2018· 桐乡一中质检 ) 下列实验方案最合理的是 ( ) A. 制备并收集 Cl 2 B. 制备氨气 C. 制备并收集 NO 2 气体 D. 制备氧气 解析 A 项中 Cl 2 的密度比空气大,收集时应用向上排空气法,应长进短出,所以错误; B 项中浓氨水滴入 CaO 中, CaO 与水反应放热,氨水受热分解,可以制取氨气,所以正确; C 项中 NO 2 能与水发生反应,不能用排水法收集,所以错误; D 项中 Na 2 O 2 为粉末状物质,不能用启普发生器的简易装置制取 O 2 ,所以错误。 答案 B 考点五:铵盐的性质 5. (2018· 嘉兴一中 ) (NH 4 ) 2 SO 4 是一种常见的化肥,某工厂用石膏、 NH 3 、 H 2 O 、 CO 2 制备 (NH 4 ) 2 SO 4 的工艺流程如下: 答案 C 考点六:工业上合成氨 6. (2017·3 月浙江绍兴一中选考科目模拟 ) 实验室模拟合成氨和氨催化氧化的流程如下: 已知实验室可用饱和亚硝酸钠 (NaNO 2 ) 溶液与饱和氯化铵溶液经加热后反应制取氮气。 (1) 从图中选择制取气体的合适装置:氮气 ________ ;氢气 ________ 。 (2) 氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有 ________ 、 ___________________________________________________________ 。 (3) 氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨, ________( “ 会 ” 或 “ 不会 ” ) 发生倒吸,原因是 _____________________________________________ 。 (4) 用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是 ____________________________ , 锥形瓶中还可观察到的现象是 ___________________________________ 。 (5) 写出乙装置中氨氧化的化学方程式: _________________________________ 。 (6) 反应结束后锥形瓶内的溶液中含有的离子为 H + 、 OH - 、 ________ 、 ________ 。 考点七:硝酸的性质 7. (2017· 北京理综, 12 ) 下述实验中均有红棕色气体产生,对比分析所得结论不正确的是 ( ) ① ② ③ A. 由 ① 中的红棕色气体,推断产生的气体一定是混合气体 B. 红棕色气体不能表明 ② 中木炭与浓硝酸产生了反应 C. 由 ③ 说明浓硝酸具有挥发性,生成的红棕色气体为还原产物 D. ③ 的气体产物中检测出 CO 2 ,由此说明木炭一定与浓硝酸发生了反应 答案 D 考点八:硝酸工业 8. (2017· 温州市 3 月选考模拟 ) 利用石灰乳吸收硝酸工业的尾气 ( 含 NO 、 NO 2 ) 反应,既能净化尾气,又能获得应用广泛的 Ca(NO 2 ) 2 ,其部分工艺流程如下: (2) 上述工艺中采用气 液逆流接触吸收 ( 尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋 ) ,其目的是 __________________________________________ ; 滤渣可循环使用,滤渣的主要成分是 ________( 填化学式 ) 。 (3) 该工艺需控制 NO 和 NO 2 物质的量之比接近 1 ∶ 1 。若 n (NO) ∶ n (NO 2 ) > 1 ∶ 1 ,则会导致 ___________________________________________________________ ; 若 n (NO) ∶ n (NO 2 ) < 1 ∶ 1 ,则会导致 _______________________________ 。 (4) 生产中溶液需保持弱碱性,在酸性溶液中 Ca(NO 2 ) 2 会发生分解,产物之一是 NO ,其反应的离子方程式为 ___________________________________ ___________________________________________________________ 。 答案 B 易错点一 氮的氧化物转化中的易错点 NO 在常温下很容易与空气中的 O 2 化合生成 NO 2 ,无色的 NO 在空气中迅速被氧化成红棕色的 NO 2 ,利用此性质可检验 NO 的存在; NO 2 溶于水生成硝酸和一氧化氮,工业上利用这一原理制取硝酸;实验室收集 NO 只能用排水法,收集 NO 2 只能用向上排空气法。 [ 易错训练 1] (2018· 浙江余姚中学高二上期末 ) 某无色混合气体中可能含有 Cl 2 、 O 2 、 SO 2 、 NO 、 NO 2 中的一种或几种。现将此混合气体通过品红溶液后,品红溶液褪色,向剩余气体中通入空气,很快变为红棕色。下列对原混合气体成分的判断正确的是 ( ) A. 肯定只有 SO 2 B. 肯定没有 Cl 2 、 O 2 和 NO 2 C. 可能有 Cl 2 和 O 2 D. 肯定只有 NO 解析 原混合气体为无色气体,故一定不含 Cl 2 和 NO 2 ,也不可能同时存在 O 2 和 NO 。混合气体通过品红溶液后,品红溶液褪色,故原混合气体中一定含有 SO 2 ;向剩余气体中通入空气,很快变为红棕色,所以原混合气体中一定含有 NO ,则一定不含 O 2 。综上所述,本题选 B 。 答案 B 易错点二 NH 3 性质认识误区 1 . 氨气与酸反应 因为氨易跟酸反应生成盐,所以不能用浓硫酸作氨气的干燥剂。同理,氨气与氯化氢气体不能共存;在中学化学中 NH 3 是唯一能与酸反应生成盐的气体;气态氢化物与最高价氧化物所对应的水化物发生化合反应,这是氮元素有别于其他元素的特征;在实验中,只有浓硝酸、浓盐酸等挥发性酸遇 NH 3 才会产生白烟,硫酸、磷酸等难挥发性酸遇 NH 3 不产生白烟现象。 2.NH 3 是中学化学中唯一能使湿润的红色石蕊试纸变蓝的气体,常用此性质检验 NH 3 的存在。 [ 易错训练 2] 氨气在工农业生产中有重要应用。 (1) ① 氮气用于工业合成氨,写出氮气的电子式: ________ ; ② NH 3 的稳定性比 PH 3 的稳定性 ________( 填 “ 强 ” 或 “ 弱 ” ) 。 (2) 如下图所示,向 NaOH 固体上滴几滴浓氨水,迅速盖上盖,观察现象。 ① 浓盐酸液滴附近会出现白烟,发生反应的化学方程式为 ___________________________________________________________ 。 铵盐 不选用的理由 NH 4 NO 3 受热分解,易发生爆炸,不安全 (NH 4 ) 2 SO 4 与 Ca(OH) 2 反应时生成 CaSO 4 呈块状,不利于 NH 3 逸出,且反应后试管难以清洗 (NH 4 ) 2 CO 3 受热分解产生 CO 2 ,导致收集到的 NH 3 不纯 3. 收集 NH 3 时,把一团干燥的棉花放在试管口,以防止与空气对流;收集完毕,尾气处理时,应放一团用稀硫酸浸湿的棉花放在试管口,以吸收 NH 3 。 [ 易错训练 3] (2016· 浙江省宁波市九所重点校高二期末 ) 某研究小组要快速制取干燥的氨气,提供的药品有:浓氨水、氯化铵固体、氢氧化钠固体、蒸馏水、碱石灰,提供的仪器如下所示 ( 必要的塞子、玻璃导管、橡胶管、固定装置和尾气处理装置略去 ) 。 (1) 需选择的药品是 ________ ,该小组选择的药品混合后快速放出氨气的原因 _________________________________________________________________________________________________ ,选择的仪器是 ______________( 填序号 ) 。 (2) 若用下图甲装置收集 NH 3 ,如何判断烧瓶中已收集满 NH 3 ? ___________________________________________________________ 。 (3) 图乙中胶头滴管中的水挤入烧瓶后,观察到的现象是 ___________________________________________________________ 。 [ 易错训练 4] 如图甲是验证铜和浓硝酸反应的装置,乙、丙是师生对实验改进后的装置: (1) 甲、乙、丙三个装置中都发生的反应的化学方程式是 ___________________________________________________________ 。 (2) 和甲装置相比,乙装置的优点是 ① __________________________ , ② ___________________________________________________________ 。 (3) 为了进一步验证 NO 2 和水的反应,某学生设计了丙装置。实验时先关闭止水夹 ________ ,再打开止水夹 ________ ,才能使 NO 2 气体充满 B 试管;当气体充满 B 试管后,将铜丝提起与溶液脱离。欲使烧杯中的水进入 B 试管,应如何操作? ___________________________________________________________ 。 解析 本题考查的是 Cu 和浓硝酸反应的装置,利用对比的方法,找出装置的优缺点,且注意 NO 2 有毒,要进行尾气吸收。再者,另一个目的是使 NO 2 与 H 2 O 反应。丙中要使 NO 2 充满 B 试管,应先关闭止水夹 c ,再打开 a 、 b , NO 2 充满试管 B 后,把铜丝拉起,然后关闭 b ,再关闭 a 后打开 c ,用手捂住试管 B ,使气体受热膨胀,与水接触, NO 2 极易与水反应,使系统内压强减小,水便进入了试管 B 。 答案 (1)Cu + 4HNO 3 ( 浓 )===Cu(NO 3 ) 2 + 2NO 2 ↑ + 2H 2 O (2) ① 可控制反应速率 ② 可吸收 NO 2 ,防止污染环境 (3)c ab 先关闭 b ,再关闭 a ,然后打开 c ,用手捂住试管 B查看更多