- 2021-07-03 发布 |
- 37.5 KB |
- 9页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2018-2019学年吉林省白城市第一中学高二下学期第二次阶段测试化学试题(Word版)
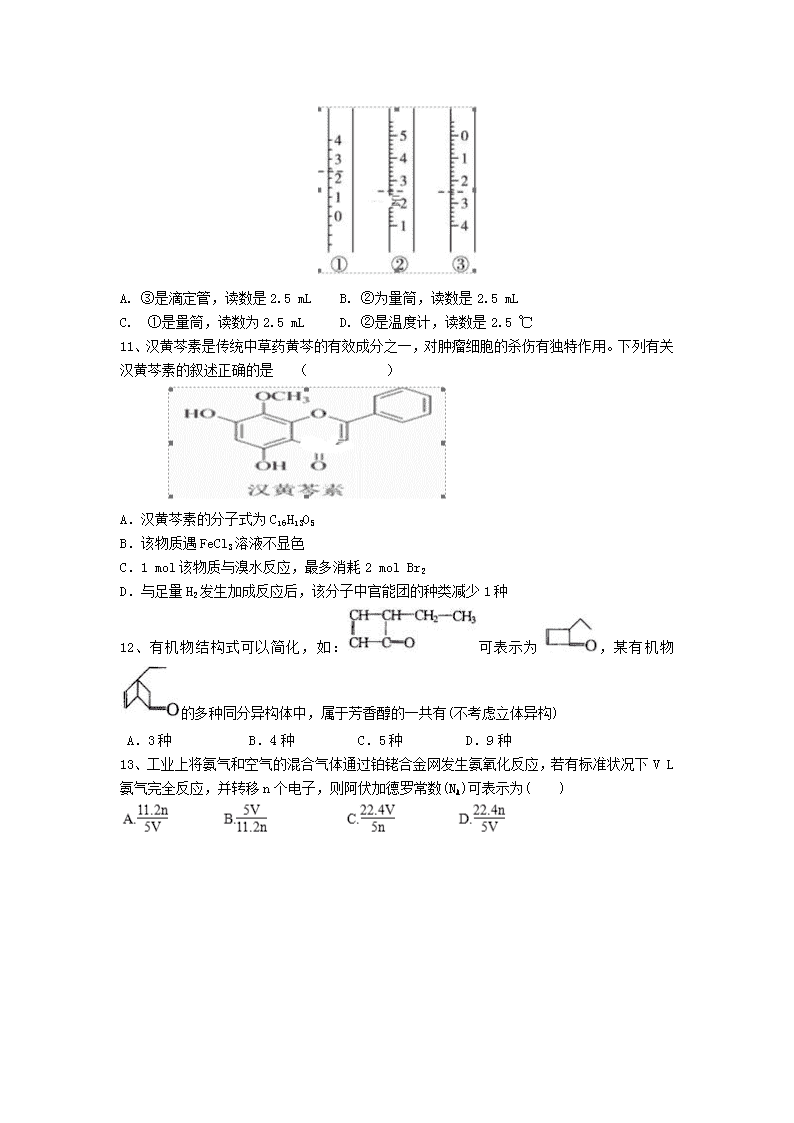
白城一中2018-2019学年度下学期第二次阶段测试 高二化学试题 可能用到的相对原子质量:H -1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 Ag-108 一、选择题(每小题只有一个正确选项,1-14题每小题2分,15-22题每小题3分,共52分) 1、设NA为阿伏伽德罗常数的值.下列叙述正确的是( ) A. 10g 46%的乙醇水溶液中所含氢原子数目为0.6NA B.常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA C.标准状况下,2.24LCH2Cl2含有分子的数目为0.1NA D.物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-离子数为NA 2、下列关于有机化合物的说法正确的是( ) A.乙烯能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色,且褪色原理相同 B.异丁烷与2—甲基丁烷互为同分异构体 C.乙苯分子中共平面的原子数最多13个 D. 乙酸和乙酸乙酯可用Na2CO3溶液加以区别 3、一氧化碳、烯烃和氢气在催化剂作用下发生烯烃的醛化反应,又称羰基的合成,如由乙烯可制丙醛:CH2=CH2+CO+H2CH3CH2CHO。由丁烯进行醛化反应也可得到醛,在它的同分异构体中,属于醛的有( ) A.2种 B.3种 C.4种 D.5种 4、下列说法正确的是 ( ) A.乳酸薄荷醇酯()仅能发生水解、氧化、消去反应 B.乙醛和丙烯醛()不是同系物,它们与氢气充分反应后的产物也不是同系物 C.碳氢质量比为3:1的有机物一定是甲烷 D.处在不同化学环境中的氢原子在核磁共振氢谱图上出现的位置不同 5、用下列实验装置进行相应实验,能达到实验目的且操作正确的是 A.用图a所示装置配制100mL0.100mol·L-1稀盐酸 B.用图b所示装置蒸干FeCl3饱和溶液制备FeCl3固体 C.用图c所示装置制取少量CO2气体 D.用图d所示装置分离CCl4萃取碘水后已分层的有机层和水层 6、下列各组物质属于同分异构体的是 A.丁烯和丁二烯 B.乙醇和乙醚 C.丙醛和丙酮 D.丙二醇和丁二醇 7、下列关于同温同压下的两种气体12C18O和14N2的判断正确的是( ) A.体积相等时密度相等 B.原子数相等时具有的中子数相等 C.体积相等时具有的电子数相等 D.质量相等时具有的质子数相等 8、下列实验中不能获得成功的是( ) A.溴苯中含有溴单质,可用NaOH溶液洗涤,再经分液而除去 B.硝基苯中混有H2SO4和HNO3,可用NaOH溶液洗涤,再经分液而除去 C.苯中的少量苯酚,可用NaOH溶液洗涤,再经分液而除去 D.苯中的少量苯酚,可加浓溴水,再经过滤而除去 9、有机物分子中原子与原子或原子与原子团间的相互影响会导致物质的化学性质不同,下列各项事实不能说明上述观点的是 A.甲苯能使KMnO4溶液褪色,甲烷不能 B.苯酚与NaOH溶液作用,乙醇不能 C.乙炔能发生加成,乙烷不能 D.甲苯苯环上氢原子比苯分子中的氢原子易被溴原子取代 10、如下图分别是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是( ) A. ③是滴定管,读数是2.5 mL B. ②为量筒,读数是2.5 mL C. ①是量筒,读数为2.5 mL D. ②是温度计,读数是2.5 ℃ 11、汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是 ( ) A.汉黄芩素的分子式为C16H13O5 B.该物质遇FeCl3溶液不显色 C.1 mol该物质与溴水反应,最多消耗2 mol Br2 D.与足量H2发生加成反应后,该分子中官能团的种类减少1种 12、有机物结构式可以简化,如:可表示为,某有机物的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构) A.3种 B.4种 C.5种 D.9种 13、工业上将氨气和空气的混合气体通过铂 铑合金网发生氨氧化反应,若有标准状况下V L氨气完全反应,并转移n个电子,则阿伏加德罗常数(NA)可表示为( ) 14、实验是化学研究的基础,下列关于各实验装置的叙述正确的是 ① ② ③ ④ A.装置①常用于分离互相溶解且沸点相差10℃以上的液态混合物 B.装置②可用于吸收NH3或HCl气体,并防止倒吸 C.装置③可用于收集H2、CO2、Cl2、NH3等气体 D.装置④可用于干燥、收集氨气,若将碱石灰改成五氧化二磷,可用于干燥、收集氯化氢 15、三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是 A.当它们的体积和温度、压强均相同时,三种气体的密度ρ(H2)>ρ(N2)>ρ(O2) B.当它们的温度和密度都相同时,三种气体的压强p(H2)查看更多