- 2021-07-02 发布 |
- 37.5 KB |
- 6页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2021高考化学一轮复习课时达标作业32化学实验方案的设计与评价含解析新人教版
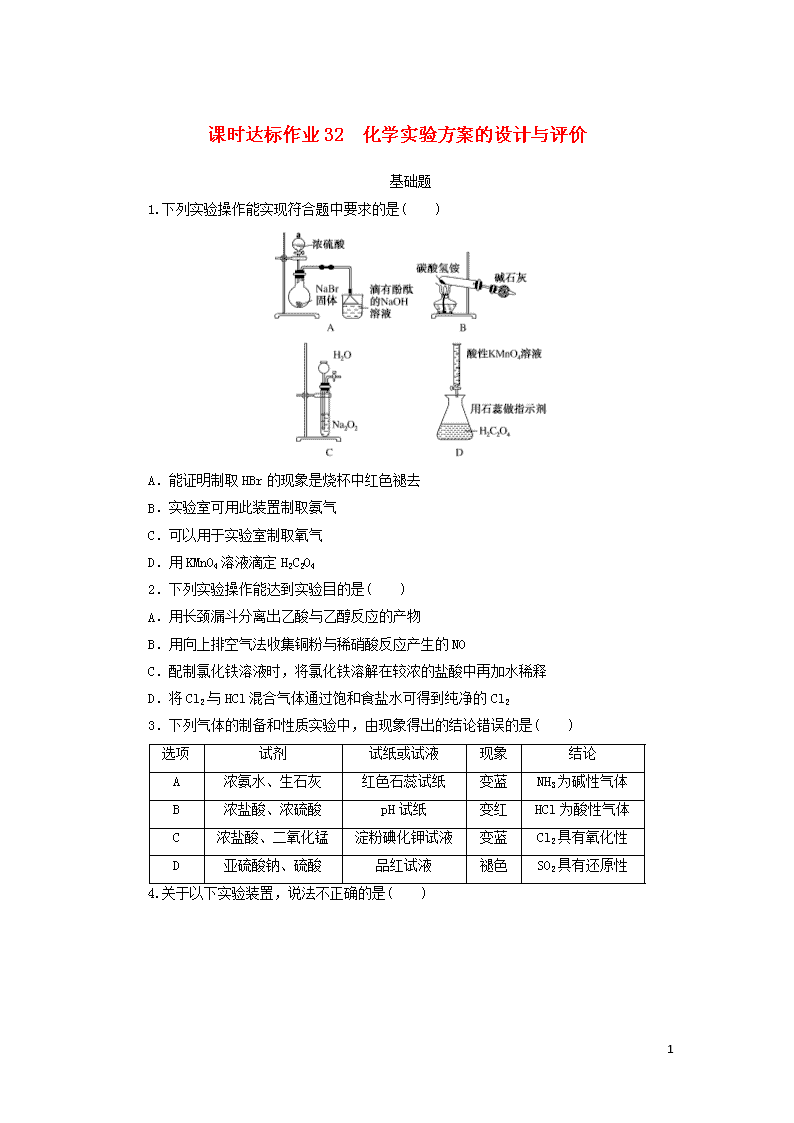
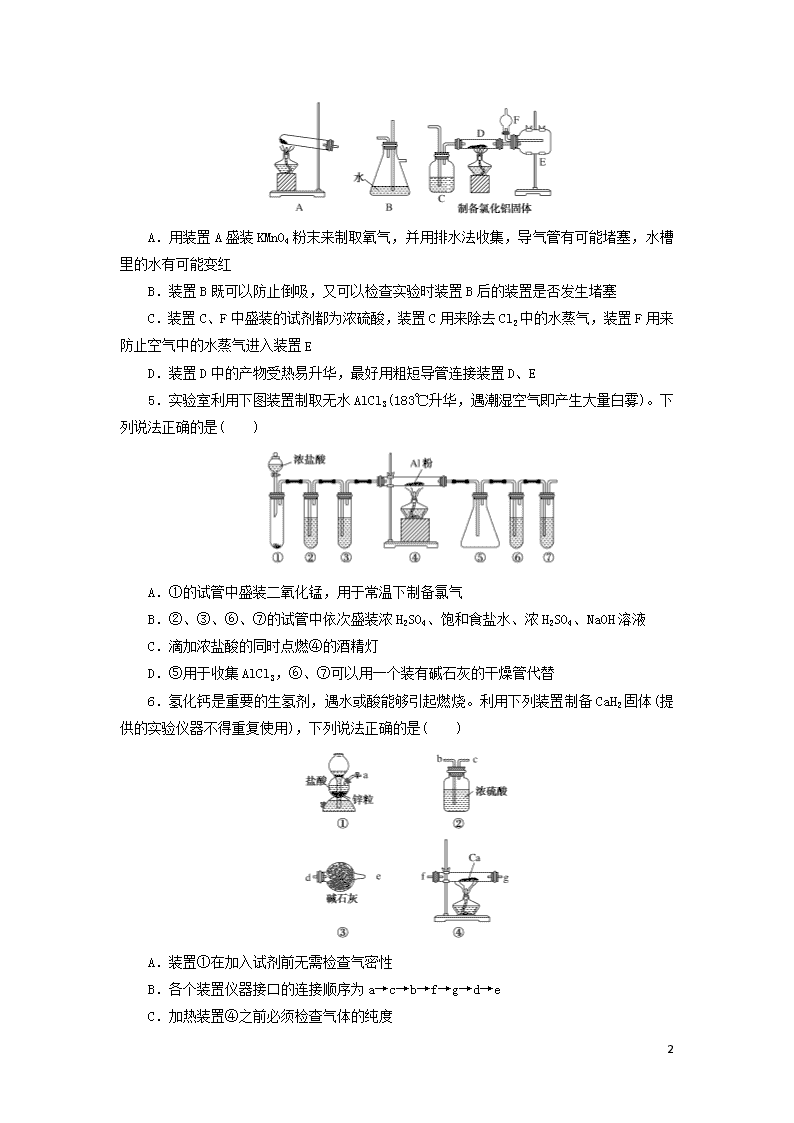
课时达标作业32 化学实验方案的设计与评价 基础题 1.下列实验操作能实现符合题中要求的是( ) A.能证明制取HBr的现象是烧杯中红色褪去 B.实验室可用此装置制取氨气 C.可以用于实验室制取氧气 D.用KMnO4溶液滴定H2C2O4 2.下列实验操作能达到实验目的是( ) A.用长颈漏斗分离出乙酸与乙醇反应的产物 B.用向上排空气法收集铜粉与稀硝酸反应产生的NO C.配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释 D.将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2 3.下列气体的制备和性质实验中,由现象得出的结论错误的是( ) 选项 试剂 试纸或试液 现象 结论 A 浓氨水、生石灰 红色石蕊试纸 变蓝 NH3为碱性气体 B 浓盐酸、浓硫酸 pH试纸 变红 HCl为酸性气体 C 浓盐酸、二氧化锰 淀粉碘化钾试液 变蓝 Cl2具有氧化性 D 亚硫酸钠、硫酸 品红试液 褪色 SO2具有还原性 4.关于以下实验装置,说法不正确的是( ) 6 A.用装置A盛装KMnO4粉末来制取氧气,并用排水法收集,导气管有可能堵塞,水槽里的水有可能变红 B.装置B既可以防止倒吸,又可以检查实验时装置B后的装置是否发生堵塞 C.装置C、F中盛装的试剂都为浓硫酸,装置C用来除去Cl2中的水蒸气,装置F用来防止空气中的水蒸气进入装置E D.装置D中的产物受热易升华,最好用粗短导管连接装置D、E 5.实验室利用下图装置制取无水AlCl3(183 ℃升华,遇潮湿空气即产生大量白雾)。下列说法正确的是( ) A.①的试管中盛装二氧化锰,用于常温下制备氯气 B.②、③、⑥、⑦的试管中依次盛装浓H2SO4、饱和食盐水、浓H2SO4、NaOH溶液 C.滴加浓盐酸的同时点燃④的酒精灯 D.⑤用于收集AlCl3,⑥、⑦可以用一个装有碱石灰的干燥管代替 6.氢化钙是重要的生氢剂,遇水或酸能够引起燃烧。利用下列装置制备CaH2固体(提供的实验仪器不得重复使用),下列说法正确的是( ) A.装置①在加入试剂前无需检查气密性 B.各个装置仪器接口的连接顺序为a→c→b→f→g→d→e C.加热装置④之前必须检查气体的纯度 6 D.装置③的主要作用是防止空气中的CO2、H2O(g)进入装置④中 能力题 7.水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解氧。实验步骤及测定原理如下: Ⅰ.取样、氧的固定 用溶解氧瓶采集水样。记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。 Ⅱ.酸化、滴定 将固氧后的水样酸化,MnO(OH)2被I-还原为Mn2+,在暗处静置5 min,然后用标准Na2S2O3溶液滴定生成的I2(2S2O+I2===2I-+S4O)。 回答下列问题: (1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是__________________________________。 (2)“氧的固定”中发生反应的化学方程式为______________________________________________。 (3)Na2S2O3溶液不稳定,使用前需标定。配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶和________;蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除________及二氧化碳。 (4)取100.00 mL水样经固氧、酸化后,用a mol·L-1 Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为______________________;若消耗Na2S2O3溶液的体积为b mL,则水样中溶解氧的含量为________mg·L-1。 (5)上述滴定完成时,若滴定管尖嘴处留有气泡会导致测定结果偏________。(填“高”或“低”) 8.为测定某氟化稀土样品中氟元素的质量分数,某化学兴趣小组进行了如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再滴定测量。实验装置如图所示。 6 (1)a的作用是________,仪器d的名称是________。 (2)检验装置气密性:________________________(填操作),关闭K,微热c,导管e末端有气泡冒出;停止加热,导管e内有一段稳定的水柱,说明装置气密性良好。 (3)c中加入一定体积高氯酸和m g氟化稀土样品,f中盛有滴加酚酞的NaOH溶液。加热b、c,使b中产生的水蒸气进入c。 ①下列物质可代替高氯酸的是________(填字母)。 A.硝酸 B.盐酸 C.硫酸 D.磷酸 ②实验中除有HF气体外,可能还有少量SiF4(易水解)气体生成。若有SiF4生成,实验结果将________(填“偏高”“偏低”或“不受影响”)。 ③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结果偏低,原因是____________________________________。 (4)向馏出液中加入V1 mL c1 mol·L-1 La(NO3)3溶液,得到LaF3沉淀,再用c2 mol·L-1 EDTA标准溶液滴定剩余La3+(La3+与EDTA按11反应),消耗EDTA标准溶液V2 mL,则氟化稀土样品中氟的质量分数为________。 (5)用样品进行实验前,需要用0.084 g氟化钠代替样品进行实验,改变条件(高氯酸用量、反应温度、蒸馏时间),测量并计算出氟元素质量,重复多次。该操作的目的是________________。 课时达标作业32 化学实验方案的设计与评价 1.解析:浓硫酸具有较强的氧化性,能把Br-氧化为Br2,溴蒸气也能使滴有酚酞的NaOH溶液褪色,A项错误;碱石灰能吸收CO2和H2O,可用此装置制取NH3,B项正确;Na2O2 6 易溶于水,且与水反应剧烈,此装置不能随意控制反应的进行,C项错误;石蕊试液由于颜色变化不明显,不易辨别,在滴定过程中不宜做指示剂,D项错误。 答案:B 2.解析:A项,乙酸和乙醇反应的产物为乙酸乙酯,乙酸乙酯不溶于水,分离应使用分液漏斗,错误;B项,NO能被空气中的氧气氧化,且其密度也与空气相近,故不能用向上排空气法收集NO,NO难溶解于水,可用排水法收集,错误;C项,氯化铁易水解,配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释可防止其水解,正确;D项,将Cl2与HCl混合气体通过饱和食盐水可除去其中的HCl,得到的Cl2中含有水蒸气,错误。 答案:C 3.解析:A.NH3制备可以采取浓氨水和生石灰制取,可用湿润的红色石蕊试纸检验,试纸变蓝则说明NH3为碱性气体,正确;B.利用浓硫酸的高沸点性,可以制取HCl气体,pH试纸变红,则说明气体为酸性气体,正确;C.浓盐酸与二氧化锰加热可以制取Cl2,Cl2可以用湿润的淀粉碘化钾试纸检验,试纸变蓝,说明KI转化为I2,则说明Cl2有强氧化性,正确;D.SO2使品红溶液褪色体现的是SO2的漂白性,错误。 答案:D 4.解析:装置A的大试管口没有塞一团棉花,故高锰酸钾粉末可能会通过导气管进入水槽中,使水槽中的水变红,并有可能堵塞导气管,A项正确;装置B后的装置发生堵塞时,会导致装置B中压强增大,从而使装置B中水面下降,长直玻璃导管中的水柱上升,因此装置B可以用于检查实验时装置B后的装置是否发生堵塞,装置B还可以用于防止倒吸,B项正确;干燥管中不能盛装浓硫酸,故C项错误;装置D中的产物受热易升华,为了防止气体凝结为固体,堵塞导管,最好用粗短导管连接装置D、E,D项正确。 答案:C 5.解析:①为氯气的发生装置,MnO2和浓盐酸在加热时才发生反应生成氯气,A项错误;制得的氯气中含有HCl和水蒸气,先通过饱和食盐水除去HCl,再通过浓硫酸除去水蒸气,④为无水AlCl3的制备装置,⑥中盛放浓硫酸,以防止空气中的水蒸气进入④中,⑦中盛放NaOH溶液,以除去未充分反应的氯气,B项错误;滴加浓盐酸,产生氯气一段时间,排出装置中的空气后,再点燃④的酒精灯,C项错误;⑤用于收集AlCl3,⑥、⑦用一个装有碱石灰的干燥管代替,既可以起到吸收未充分反应的氯气的作用,也可以防止空气中的水蒸气进入④中,D项正确。 答案:D 6.解析:装置①为启普发生器,加入试剂之前必须检查装置的气密性,A项错误;装置①中产生的氢气会混有HCl、H2 6 O(g),通过装置③可以除去这两种杂质,所以仪器接口的连接顺序为a→d→e→f→g(或g→f)→b→c,B项错误;为了防止金属钙与空气中的物质发生反应,需要在加热前通入氢气排尽装置④硬质玻璃管中的空气,通过检查氢气的纯度确定是否将空气排尽,C项正确;装置③的作用是除去氢气中混有的HCl、H2O(g),D项错误。 答案:C 7.解析:本题采用碘量法测定水中的溶解氧的含量,属于氧化还原滴定。(2)根据氧化还原反应原理,Mn(OH)2被氧气氧化为MnO(OH)2,由此可得方程式为2Mn(OH)2+O2===2MnO(OH)2。(3)一定物质的量浓度溶液的配制还需要量筒;加热可以除去溶解的氧气,避免实验结果不准确。(4)该实验用硫代硫酸钠标准液滴定I2,因此终点现象为当最后一滴标准液滴入时,溶液由蓝色变为无色,且半分钟内无变化;根据关系式O2~2MnO(OH)2~2I2~4Na2S2O3可得水样中溶解氧的含量为[(ab×10-3)mol÷4×32 g·mol-1×103 mg·g-1]÷0.1 L=80ab mg·L-1。(5)终点读数时有气泡,气泡占据液体应占有的体积,会导致测得的消耗的Na2S2O3体积偏小,使最终结果偏低。 答案:(1)使测定值与水体中的实际值保持一致,避免产生误差 (2)2Mn(OH)2+O2===2MnO(OH)2 (3)量筒 氧气 (4)当最后一滴标准液滴入时,溶液由蓝色变为无色,且半分钟内无变化 80ab (5)低 8.解析:(1)a的作用是平衡压强,防止圆底烧瓶中压强过大,引起爆炸。仪器d的名称是直形冷凝管。(2)检查装置气密性时在b和f中加水,使水浸没a和e的末端,从而形成密闭体系。(3)①此实验是利用高氯酸(高沸点酸)将样品中的氟元素转化为HF(低沸点酸)蒸出。硝酸和盐酸易挥发,A、B两项错误;硫酸和磷酸沸点高,难挥发,C、D两项正确。 答案:(1)平衡压强 直形冷凝管 (2)在b和f中加水,水浸没导管a和e末端 (3)①CD ②不受影响 ③充分吸收HF气体,防止其挥发损失 (4) (5)寻找最佳实验条件 6查看更多