- 2021-07-02 发布 |
- 37.5 KB |
- 12页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2017-2018学年河南省辉县市第一高级中学高二下学期第一次阶段性测试化学(培优班)试题(Word版)
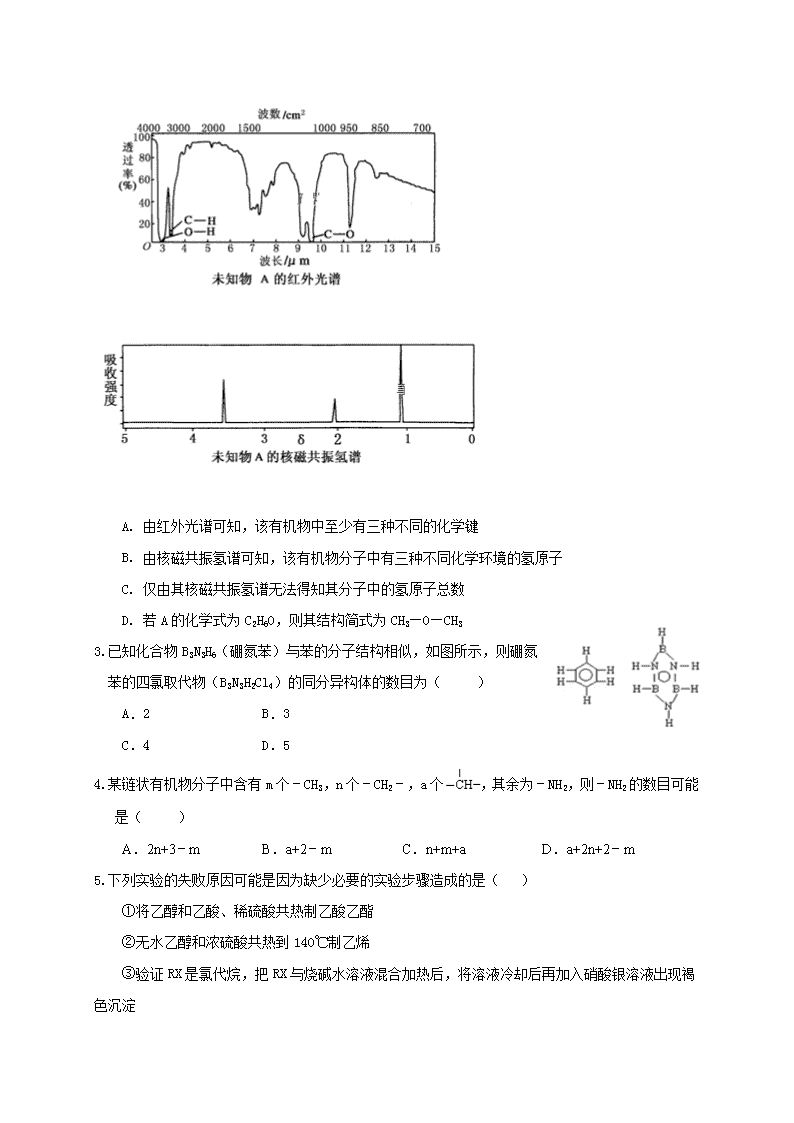
辉县市一中2017——2018学年下期第一次阶段性考试 高二(培优班)化学试卷 命题人:王智明 注意事项: 1.答题前填写好自己的姓名、班级、考号等信息 2.请将答案正确填写在答题卡上,在试卷上作答无效 可能用到的相对原子质量:C-12 H-1 O-16 Mg-24 Cl-35.5 N-14 Cu-64 第Ⅰ卷(选择题,共51分) 一、选择题(每题3分,共48分) 1.下列说法正确的是( ) A.按系统命名法, 的名称为2,5,6﹣三甲基﹣4﹣乙基庚烷 B.常压下,正戊烷、异戊烷、新戊烷的沸点依次增大 C.肌醇 与葡萄糖的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 D.1.0 mol的 最多能与含5.0 molNaOH的水溶液完全反应 2.已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中错误的是( ) A. 由红外光谱可知,该有机物中至少有三种不同的化学键 B. 由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子 C. 仅由其核磁共振氢谱无法得知其分子中的氢原子总数 D. 若A的化学式为C2H6O,则其结构简式为CH3—O—CH3 3.已知化合物B3N3H6(硼氮苯)与苯的分子结构相似,如图所示,则硼氮苯的四氯取代物(B3N3H2Cl4)的同分异构体的数目为( ) A.2 B.3 C.4 D.5 4.某链状有机物分子中含有m个﹣CH3,n个﹣CH2﹣,a个,其余为﹣NH2,则﹣NH2的数目可能是( ) A.2n+3﹣m B.a+2﹣m C.n+m+a D.a+2n+2﹣m 5.下列实验的失败原因可能是因为缺少必要的实验步骤造成的是( ) ①将乙醇和乙酸、稀硫酸共热制乙酸乙酯 ②无水乙醇和浓硫酸共热到140℃制乙烯 ③验证RX是氯代烷,把RX与烧碱水溶液混合加热后,将溶液冷却后再加入硝酸银溶液出现褐色沉淀 ④做醛的还原性实验时,当加入新制的氢氧化铜悬浊液后,未出现红色沉淀 ⑤检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,加入银氨溶液水浴加热后未析出银镜 A.①③④⑤ B.③④⑤ C.③⑤ D.全部 6.利用下图所示的有机物X可生产S﹣诱抗素Y.下列说法正确的是( ) 一定条件 A.Y既可以与FeCl3溶液发生显色反应,又可使酸性KMnO4溶液褪色 B.1mol Y与足量NaOH溶液反应,最多消耗3mol NaOH C.1mol X最多能加成9mol H2 D.X可以发生氧化、取代、酯化、加聚、缩聚反应 7.某烃的结构简式为,分子中处于四面体结构中心的碳原子(即饱和碳原子)数为a,可能在同一平面内的碳原子数最多为b,一定在同一直线上的碳原子数最多为c,则a、b、c依次为( ) A.3、12、8 B.4、13、4 C.3、12、4 D.4、13、8 8.0.1mol某烃完全燃烧时生成30.8gCO2和12.6gH2O,且能使酸性高锰酸钾溶液褪色,若其结构中只含有两个﹣CH3,则该物质的结构(不考虑顺反异构)最多有( ) A.6种 B.8种 C.7种 D.10种 9.2015年诺贝尔生理学或医学奖的一半授予我国药物化学家屠吆吆,以表彰她发明抗疟疾新药青蒿素和双氢青蒿素.以异胡薄荷醇为起始原料是人工全合成青蒿素的途径之一(如图).下列说法正确的是( ) A.异胡薄荷醇的分子式为C10H17O B.异胡薄荷醇在NaOH醇溶液中可发生消去反应 C.青蒿素分子中含有7个手性碳原子 D.青蒿素在热的酸、碱溶液中均可稳定存在 10.黄曲霉毒素M1是一种具有强致癌性的有机物,其分子结构如图所示.下列有关黄曲霉毒素M1的说法正确的是( ) A.黄曲霉毒素M1的分子式为C17H14O7 B.黄曲霉毒素M1含有羟基,此羟基能被催化氧化为醛基 C.1mol黄曲霉毒素M1与NaOH溶液发生反应最多能消耗2molNaOH D.1mol黄曲霉毒素M1最多能与7molH2发生加成反应 11.药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得: 下列有关叙述正确的是( ) A.贝诺酯分子中有三种含氧官能团 B.可用FeCl3 溶液区别乙酰水杨酸和对乙酰氨基酚 C.乙酰水杨酸和对乙酰氨基酚均能与NaHCO3 溶液反应 D.贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠 12.有机物分子中,当某个碳原子连接着四个不同的原子或原子团时,这种碳原子称为“手性碳原子”.例如,如图有机物分子中带“*”碳原子就是手性碳原子.该有机物分别发生下列反应,生成的有机物分子中仍含有手性碳原子的是( ) A.与乙酸发生酯化反应 B.与NaOH水溶液反应 C.与银氨溶液作用只发生银镜反应 D.催化剂作用下与H2反应 13.尿黑酸是由酪氨酸在人体内非正常代谢而产生的一种物质。其转化过程如下: 下列说法错误的是( ) A.对羟基苯丙酮酸分子中在同一平面上的碳原子至少有7个 B.1 mol尿黑酸与足量浓溴水反应,最多消耗3molBr2 C.酪氨酸既能与盐酸反应,又能与氢氧化钠反应 D.1 mol尿黑酸与足量NaHCO3反应,最多消耗3 molNaHCO3 14.如图为某有机物的结构简式。已知酯类在铜铬氧化物(CuO·CuCrO4)催化下,与氢气反应得到醇,羰基双键可同时被还原,但在催化氢化过程中苯环不变,其反应原理如下:在铜铬氧化物催化下,R1COOR2+2H2→R1CH2OH+R2OH关于该化合物的下列说法中,正确的是( ) A.该有机物的化学式为C20H14O5,该有机物可以属于酯类、酚类、醚类 B.该有机物遇浓溴水发生加成反应 C.与足量氢氧化钠溶液充分反应,1mol该有机物最多可以与5molNaOH反应,所得产物中有醇类物质 D.1mol该有机物在铜铬氧化物催化下仅能与2mol氢气发生反应 15.α,β,γ和δ四种生育三烯酚是构成维生素E的主要物质,下列叙述中不正确的是( ) A.α和δ两种生育三烯酚互为同系物,β和γ两种生育三烯酚互为同分异构体 B.四种生育三烯酚均可使酸性高锰酸钾溶液及溴的四氯化碳溶液褪色 C.α-生育三烯酚分子中一定在同一平面内的最多的碳原子数为10 D.四种生育三烯酚的结构中均不存在手性碳原子 16.现有一多肽,其化学式为C55H70O19N10,将其彻底水解后只得到下列四种氨基酸: 甘氨酸(H2N—CH2COOH),丙氨酸(),苯丙氨酸() 谷氨酸(),则该多肽中所含肽键的数目以及水解后得到的谷酸和苯氨酸的数目分别是( ) A.10,4,3 B.10,3,4 C.9,4,3 D.9,3,4 二、填空题(共52分) 17.(8分)糠酸又称呋喃甲酸,在食品工业作防腐剂,还可用于合成树脂或医药、香料等的中间体。以米槺或玉米芯提取的呋喃甲醛为原料合成糠酸反应如下 几种有机物性质如下: 名称 性状 相对分 子质量 溶解度 冷水 热水 乙醇 乙醚 呋喃甲醛 无色液体 96 微溶 易溶 易溶 互溶 呋喃甲醇 无色液体 98 互溶 互溶 易溶 易溶 呋喃甲酸 无色晶体 112 微溶 易溶 可溶 易溶 刚果红试纸pH变色范围:3.0(蓝紫色)~5.0(红色) 呋喃甲酸的实验室制备方法如下: 三颈瓶中放入3.28mL(0.04mol)新蒸呋喃甲醛,控温8~12℃下滴加4mL40%NaOH溶液,并磁力搅拌回流30分钟。向反应混合物滴加蒸馏水(约15mL)使其恰好澄清,用50mL 乙醚萃取分液,其水溶液用水蒸气蒸馏,弃去镏出物,慢慢滴加2:1盐酸到pH=3,搅拌,析出结晶,抽滤并用少量水洗涤抽干,得精产品1.75g。 回答以下问题: (1)三颈瓶中反应需要搅拌回流30分钟的原因是__________。 (2)呋喃甲醛在碱中反应大量放热,实验中需要控温8-12℃,其操作方法_________。 (3)50mL乙醚萃取分液,除去呋喃甲醇的操作方法是____________。 A、直接用50mL乙醚萃取分液 B、将溶液分两份,乙醚也分两份,分别萃取,萃取液合并 C、先用30mL乙醚萃取分液,再分别州l0mL乙醚萃取两次,并将三次萃取液合并 (4)乙醚提取后的水溶液要用盐酸酸化。配制100mL 2:1稀盐酸(水与盐酸体积比)的方法是___________;判断盐酸加入足量的方法是________________。 (5)乙醚易挥发、易燃,蒸气可使人失去知觉,在蒸馏回收乙醚时注意:_____________;水蒸气蒸馏的方法应选择________(填字母序号); (6)计算呋喃甲酸的产率___________________。 18.(12分)原油价格的下跌,加剧能源的过度开采,因此更要开展汽油的有机合成的研究。以下是一种合成汽油的路线: 已知: (1)在反应①—⑥中,属于加成反应的是 。 (2)A中官能团名称为 ,系统命名法命名 E 的名称为 。 (3)写出下列反应方程式 E→F ; H→G 。 (4)H 也能与NaOH 溶液反应,其反应方程式为: 。 19.(16分)对氨基苯甲酸酯类是一类局部麻醉药,化合物M是该类药物之一。合成M的一种路线如下: 已知以下信息: ①核磁共振氢谱显示B只有一种化学环境的氢,H苯环上有两种化学环境的氢。 ② 。 ③E为芳香烃,其相对分子质量为92。 ④(苯胺,易被氧化)。 回答下列问题: (1)A的结构简式为_________________,其化学名称是 。 (2)由E生成F的化学方程式为_________________________________________。 (3)由G生成H的反应类型为__________________,H在一定条件下可以发生聚合反应,写出该聚合反应的化学方程式___________________________________________。 (4)M的结构简式为________________________________。 (5)D的同分异构体中不能与金属钠反应生成氢气的共有_________种(不考虑立体异构),其中核磁共振氢谱只有两组峰,且峰面积比为6:1的是______________(写结构简式)。 20.(16分)有机物F是一种香料,其合成路线如图所示: (1)A的名称为 ,试剂X的结构简式为 ,步骤Ⅵ的反应类型为 。 (2)步骤Ⅰ的反应条件分别为 。 (3)步骤Ⅱ反应的化学方程式为 。 (4)满足括号中条件(①苯环上只有两个取代基,②能与FeCl3溶液发生显色反应,③能发生水解反应和银镜反应)的E的同分异构体有 种,其中核磁共振氢谱峰面积比为6︰2︰2︰1︰1的分子的结构简式为 。 (5)依据题中信息,完成以为原料制取的合成路线图。 合成路线图示例如下: 辉县市一中2017——2018学年下期第一次阶段性考试 高二(培优班)化学试卷 参考答案 一、选择题 1—5DDCBB 6—10DBBCC 11—16BCDCDC 二、填空题 17.(1)呋喃甲醛微溶于水,搅拌充分混合加快反应速率 (其它合理答案均给分) (2)冷水浴 (冰水浴,其它合理答案均给分) (3)C (4)用量筒分别量取66ml水、34ml浓盐酸,于烧杯中混合,用玻璃棒搅拌均匀 (其它合理答案均给分) 使用刚果红试纸测定溶液pH,当试纸变蓝紫色时,说明加入盐酸足量 (上层清液中继续滴加盐酸,不产生浑浊,说明盐酸加入足量。其它合理答案均给分) (5)在水浴上进行蒸馏,切忌直接明火加热。(其它合理答案均给分) C (6)78.1% 18(1)①③⑤ (2)醛基 2-甲基-1-丙醇 (3) (4) 19.(1) 2-甲基丙烯 (2) (3)还原反应 n +(n—1)H2O (4) (5)15 20.(1)甲苯;CH3CHClCOOH;取代(或酯化)反应; (2)光照; (3)C6H5-CH2Cl + NaOH C6H5-CH2OH + NaCl; (4)15;; (5)查看更多